
|
| |
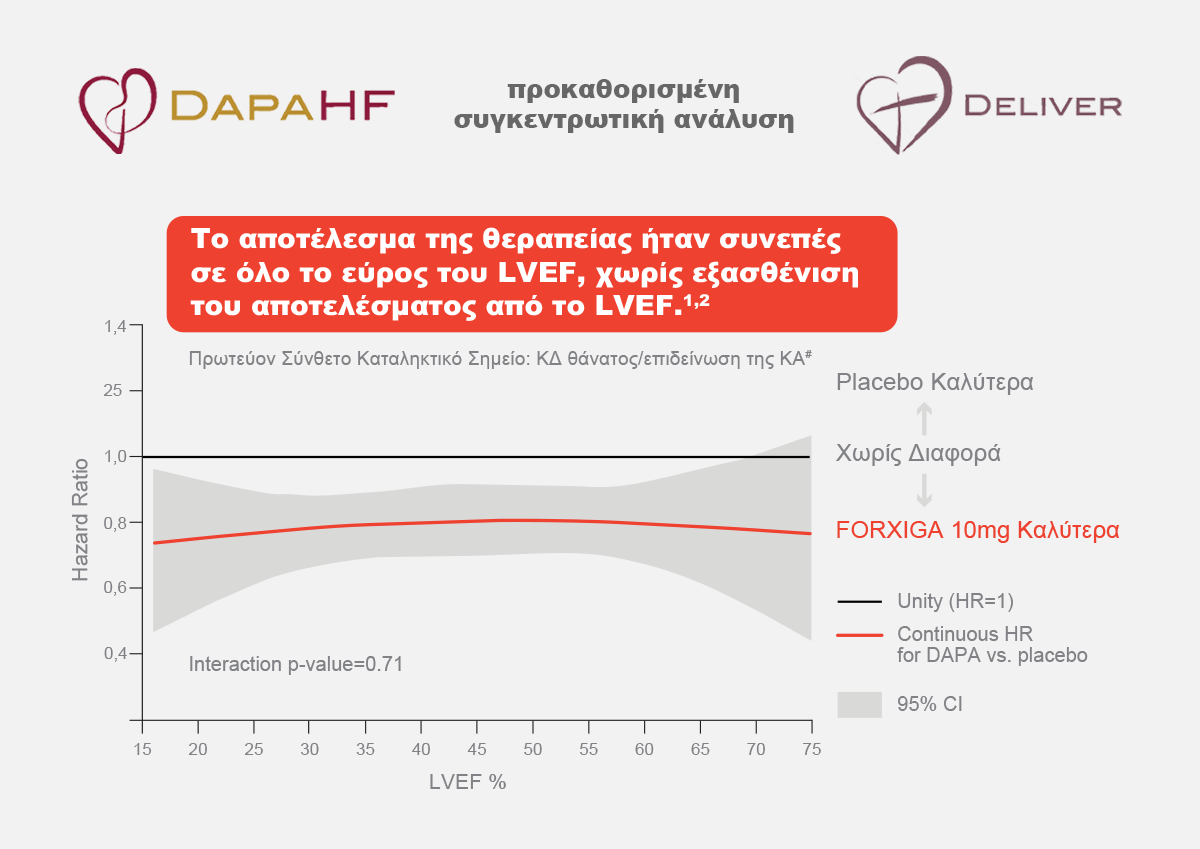
Το Forxiga 10mg στην συγκεντρωτική ανάλυση των μελετών DAPA-HF & DELIVER απέδειξε στατιστικά σημαντικό όφελος στη μείωση του κινδύνου για ΚΔ θάνατο ή επιδείνωση της ΚΑ#
σε όλο το εύρος του κλάσματος εξώθησης1,2
|
|
|
|
| |
Ανεπιθύμητες ενέργειες σε ελεγχόμενες με εικονικό φάρμακο κλινικές μελέτες και εμπειρία μετά την κυκλοφορία1
|
|
|
|
|
| |
| |
α Ο πίνακας παρουσιάζει δεδομένα για μια περίοδο διάρκειας έως και 24 εβδομάδων (βραχείας διάρκειας) ανεξαρτήτως θεραπείας διάσωσης για την επίτευξη γλυκαιμικού ελέγχου. β Βλέπε αντίστοιχη υποπαράγραφο παρακάτω για επιπρόσθετες πληροφορίες. γ Ο όρος αιδοιοκολπίτιδα, βαλανίτιδα και σχετιζόμενες λοιμώξεις των γεννητικών οργάνων περιλαμβάνει π.χ., τους προκαθορισμένους προτιμώμενους όρους: αιδοιοκολπική μυκητιασική λοίμωξη, κολπική λοίμωξη, βαλανίτιδα, μυκητιασική λοίμωξη των γεννητικών οργάνων, αιδοιοκολπική καντιντίαση, αιδοιοκολπίτιδα, καντιντιασική βαλανίτιδα, καντιντίαση γεννητικών οργάνων, λοίμωξη ανδρικών γεννητικών οργάνων, λοίμωξη του πέους, αιδοιίτιδα, βακτηριακή κολπίτιδα, απόστημα του αιδοίου. δ Ο όρος ουρολοίμωξη περιλαμβάνει τους ακόλουθους προτιμώμενους όρους, που παρατίθενται κατά σειρά αναφερόμενης συχνότητας: ουρολοίμωξη, κυστίτιδα, ουρολοίμωξη από κολοβακτηρίδιο, λοίμωξη του ουροποιογεννητικού συστήματος, πυελονεφρίτιδα, φλεγμονή του κυστικού τριγώνου, ουρηθρίτιδα, λοίμωξη του νεφρού και προστατίτιδα. ε Ο όρος μειωμένος ενδαγγειακός όγκος περιλαμβάνει, π.χ., τους προκαθορισμένους προτιμώμενους όρους: αφυδάτωση, υποογκαιμία, υπόταση. στ Ο όρος πολυουρία περιλαμβάνει τους προτιμώμενους όρους: πολλακιουρία, πολυουρία, αυξημένη αποβολή ούρων. ζ Οι μέσες μεταβολές του αιματοκρίτη από την αρχική τιμή ήταν 2,30% για τη δαπαγλιφλοζίνη 10mg έναντι 0,33% για το εικονικό φάρμακο. Τιμές αιματοκρίτη >55% αναφέρθηκαν σε 1,3% των ατόμων που έλαβαν δαπαγλιφλοζίνη 10 mg έναντι 0,4% των ατόμων υπό εικονικό φάρμακο. η Η μέση ποσοστιαία μεταβολή από την αρχική τιμή για τη δαπαγλιφλοζίνη 10 mg έναντι του εικονικού φαρμάκου, αντίστοιχα, ήταν: ολική χοληστερόλη 2,5% έναντι 0,0%, χοληστερόλη HDL 6,0% έναντι 2,7%, χοληστερόλη LDL 2,9% έναντι 1,0%, τριγλυκερίδια 2,7% έναντι 0,7%. θ Βλέπε ενότητα 4.4. ι Η ανεπιθύμητη ενέργεια ταυτοποιήθηκε μέσω παρακολούθησης μετά την κυκλοφορία. Το εξάνθημα περιλαμβάνει τους ακόλουθους προτιμώμενους όρους, που καταγράφηκαν κατά σειρά συχνότητας σε κλινικές μελέτες: εξάνθημα, εξάνθημα γενικευμένο, εξάνθημα κνησμώδες, εξάνθημα κηλιδώδες, εξάνθημα κηλιδοβλατιδώδες, εξάνθημα φλυκταινώδες, εξάνθημα φυσαλλιδώδες και εξάνθημα ερυθηματώδες. Σε κλινικές μελέτες ελεγχόμενες με δραστικό και εικονικό φάρμακο (δαπαγλιφλοζίνη, Ν=5.936, όλοι οι έλεγχοι, Ν=3.403), η συχνότητα εξανθήματος ήταν παρόμοια για τη δαπαγλιφλοζίνη (1,4%) και για όλους τους έλεγχους (1,4%), αντίστοιχα. κ Η συχνότητα ανεπιθύμητων ενεργειών ταυτοποιήθηκε από τον πλήρη πληθυσμό της μελέτης σε 2 ελεγχόμενες με εικονικό φάρμακο μελέτες σε άτομα με σακχαρώδη διαβήτη τύπου 1. λ Αναφέρθηκε στη μελέτη καρδιαγγειακών εκβάσεων σε ασθενείς με διαβήτη τύπου 2 (DECLARE). Η συχνότητα βασίζεται σε ετήσιο ποσοστό.
|
|
|
| |
| |
| |
Σχεδιασμός Μελέτης DAPA-HF
Η μελέτη DAPA-HF είναι διεθνής, πολυκεντρική, παράλληλων ομάδων, τυχαιοποιημένη, διπλά τυφλή μελέτη σε ασθενείς με χρόνια καρδιακή ανεπάρκεια με μειωμένο κλάσμα εξώθησης που μελετά την επίδραση της δαπαγλιφλοζίνης 10mg συγκρινόμενη με το εικονικό φάρμακο επιπλέον της καθιερωμένης θεραπείας.
Σχεδιασμός Μελέτης Deliver
Η μελέτη DELIVER είναι διεθνής, πολυκεντρική, παράλληλων ομάδων, τυχαιοποιημένη, διπλά τυφλή μελέτη σε ασθενείς με χρόνια καρδιακή ανεπάρκεια με ήπια μειωμένο ή διατηρημένο κλάσμα εξώθησης που μελετά την επίδραση της δαπαγλιφλοζίνης 10mg συγκρινόμενη με το εικονικό φάρμακο επιπλέον της καθιερωμένης θεραπείας.
Σε μια συγκεντρωτική ανάλυση των μελετών DAPA‑HF και DELIVER, η αναλογία κινδύνου (HR) για τη δαπαγλιφλοζίνη έναντι του εικονικού φαρμάκου στο σύνθετο καταληκτικό σημείο καρδιαγγειακού θανάτου, νοσηλείας για καρδιακή ανεπάρκεια ή επείγουσας επίσκεψης για καρδιακή ανεπάρκεια ήταν 0,78 (95% CI 0,72, 0,85), p<0,0001. Το αποτέλεσμα της θεραπείας ήταν συνεπές σε όλο το εύρος του LVEF, χωρίς εξασθένιση του αποτελέσματος από το LVEF. Σε μια προκαθορισμένη συγκεντρωτική ανάλυση σε επίπεδο ασθενών των μελετών DAPA‑HF και DELIVER, η δαπαγλιφλοζίνη σε σύγκριση με το εικονικό φάρμακο μείωσε τον κίνδυνο καρδιαγγειακού θανάτου (HR 0,85 [95% CI 0,75, 0,96], p=0,0115). Και οι δύο μελέτες συνέβαλαν στο αποτέλεσμα.
|
|
|
| |
|
|
| |
| |
#Επιδείνωση ΚΑ: Περιλαμβάνει νοσηλεία για καρδιακή ανεπάρκεια ή επείγουσα επίσκεψη για καρδιακή ανεπάρκεια (μη προγραμματισμένη εκτίμηση από γιατρό, χρήζουσα θεραπείας για την επιδείνωση της καρδιακής ανεπάρκειας άλλη από μόνο μια αύξηση στη δόση των από στόματος διουρητικών).
ΚΔ: Καρδειαγγειακός, ΚΑ: Καρδιακή ανεπάρκεια, LVEF: Left Ventricular Ejection Fraction, HR: Hazard Ratio, CI: Confidence Interval.
Forxiga 10mg Θεραπευτικές ενδείξεις
Σακχαρώδης διαβήτης τύπου 2
Το Forxiga ενδείκνυται για χρήση σε ενήλικες και παιδιά ηλικίας 10 ετών και άνω για τη θεραπεία του ανεπαρκώς ελεγχόμενου σακχαρώδη διαβήτη τύπου 2 ως συμπληρωματική θεραπεία στη δίαιτα και την άσκηση:
- ως μονοθεραπεία, όταν η μετφορμίνη θεωρείται ακατάλληλη λόγω δυσανεξίας.
- επιπρόσθετα με άλλα φαρμακευτικά προϊόντα για τη θεραπεία του διαβήτη τύπου 2.
Καρδιακή ανεπάρκεια
Το Forxiga ενδείκνυται για χρήση σε ενήλικες ασθενείς για τη θεραπεία της συμπτωματικής χρόνιας καρδιακής ανεπάρκειας.
Χρόνια νεφρική νόσος
Το Forxiga ενδείκνυται για χρήση σε ενήλικες ασθενείς για τη θεραπεία της χρόνιας νεφρικής νόσου.
ΒΙΒΛΙΟΓΡΑΦΙΑ:
1. Forxiga 10mg, Περίληψη Χαρακτηριστικών Προϊόντος Ιανουάριος 2024
2. Jhund PS et al Nat Med. 2022 Sep;28(9):1956-1964. doi: 10.1038/s41591-022-01971-4
|
|
|
| |
|
|
| |
Χορηγείται με ιατρική συνταγή
Forxiga F.C.Tab 10mg/tab Btx28
Λ.T. 43,26€, Χ.Τ. 31,39€, Ν.Τ. 27,30€
|

|
|
|
|
|
| |
| |
Το μήνυμα εστάλη από την AstraZeneca αποκλειστικά και μόνο για προσωπική σας χρήση και απαγορεύεται οποιαδήποτε προώθηση, κοινοποίηση ή διάθεση του περαιτέρω.
Η AstraZeneca δεσμεύεται ως προς την ποιότητα και την εγκυρότητα των πληροφοριών που παρατίθενται στο παρόν newsletter, υπό την επιφύλαξη τυχόν τεχνικών ή τυπογραφικών λαθών που δεν μπορούν να προβλεφθούν ή έχουν προκύψει ακούσια ή λόγω διακοπών λειτουργίας της παρούσας ιστοσελίδας για λόγους ανωτέρας βίας.
Σας ενημερώνουμε ότι η AstraZeneca, κατόπιν σχετικής συναίνεσης σας, τηρεί αρχείο και επεξεργάζεται τα προσωπικά σας δεδομένα (ονοματεπώνυμο, ιδιότητα, τηλέφωνο επικοινωνίας, διεύθυνση ηλεκτρονικού ταχυδρομείου (e-mail)), με σκοπό την αποστολή προς εσάς υλικού ιατρικής ενημέρωσης και την ενημέρωσή σας για τις επιστημονικές εκδηλώσεις που διοργανώνει. Η AstraZeneca χειρίζεται τα παραπάνω προσωπικά σας δεδομένα καθώς και όποια επιπλέον της κοινοποιήσετε με πλήρη σεβασμό και με βάση τα όσα προβλέπει το κείμενο κανονιστικό και νομοθετικό πλαίσιο περί προστασίας δεδομένων προσωπικού χαρακτήρα, διατηρώντας πάντα το δικαίωμα περί πρόσβασης σας στα τηρούμενα από αυτήν προσωπικά σας δεδομένα. Οποιαδήποτε πληροφορία μας παρέχετε, συμπεριλαμβανομένων ανεπιθύμητων ενεργειών ή ποιοτικών παραπόνων, ενδέχεται να διαβιβαστεί στις κανονιστικές και ρυθμιστικές αρχές, σε θυγατρικές μας εταιρείες ή/και σε επιχειρηματικούς εταίρους με τους οποίους συνδεόμαστε συμβατικά. Τα άτομα αυτά ενδέχεται να βρίσκονται σε διαφορετική χώρα από τη δική σας. Για περισσότερες πληροφορίες σχετικά με την αναθεωρημένη πολιτική απορρήτου της AstraZeneca, παρακαλούμε
πατήστε εδώ.
Αν επιθυμείτε να διαγραφείτε από τη λίστα μπορείτε να αποστείλετε το αίτημα σας στην ηλεκτρονική διεύθυνση
georgios.christias@astrazeneca.com
με θέμα "Διαγραφή από τη λίστα παραληπτών newsletter". Το αρμόδιο πρόσωπο της AstraZeneca προς το οποίο μπορείτε να απευθύνεστε προκείμενου να ασκήσετε το δικαίωμά σας περί ενημέρωσης, πρόσβασης και αντίρρησης στην επεξεργασία των προσωπικών σας δεδομένων είναι ο κος Γεώργιος Χρηστιάς (τηλέφωνο επικοινωνίας
210-6871500, διεύθυνση ηλεκτρονικού ταχυδρομείου:
georgios.christias@astrazeneca.com).
Τέλος, για τις ανάγκες ιατρικής πληροφόρησης, σας ενημερώνουμε ότι μπορείτε είτε να επισκεφτείτε τον ιστότοπο του τμήματος Ιατρικής Πληροφόρησης της AstraZeneca Ελλάδος:
https://medicalinformation.astrazeneca.gr/ είτε να επικοινωνήσετε στο τηλέφωνο
0030 210-6871500.
Copyright 2024 AstraZeneca
|
|
|
| |
|
|
| |
| |
FOR/00420/1/0224
exp.date: 02/2026
|
|
|
| |
|
|